Waarom zouden we streven naar 800 kilometer? Omdat deze waarde de hoogst verwachte waarde is voor het cruisebereik van de meeste mensen, als het cruisebereik van het elektrische voertuig niet 800 kilometer kan bereiken en de kosten door de meeste mensen kunnen worden geaccepteerd, zal het elektrische voertuig minder populariteit hebben. Dus hebben we deze waarde ingesteld op het doel van ons Battery 500 -project. Het project begon in 2009 en wordt gedomineerd door het Almaden Research Center. Sindsdien heeft IBM dit onderzoek uitgevoerd met een aantal zakelijke partners en onderzoeksinstituten uit Europa, Azië en de Verenigde Staten. Het Battery 500-project is gebaseerd op metaal-luchttechnologie. In vergelijking met lithiumbatterijen hebben metalen batterijen meer energie per massa-eenheid. Het projectonderzoek duurt nog steeds enkele jaren om te worden gecommercialiseerd. Maar door deze zeven jaar van experimenten kunnen we denken dat de toekomstige metal-luchtbatterij inderdaad nuttig is in elektrische voertuigen. Waarom is het een metalen batterij? Als ik lithium-luchtbatterijen als voorbeeld neemt om dit probleem te begrijpen, laten we eerst kijken naar het verschil tussen lithium-ionbatterijen (nu gemeenschappelijke lithiumbatterijen) en lithium-luchtbatterijen. De onderstaande afbeelding toont de interne toestand van de batterij tijdens het opladen en ontladen van de lithium -ionbatterij. In een conventionele lithiumionbatterij is de positieve elektrode koolstof en bestaat de negatieve elektrode uit verschillende overgangsmetaaloxiden zoals kobalt, nikkel, mangaan en dergelijke. Beide elektroden werden ondergedompeld in een elektrolyt waarin een lithiumzout werd opgelost. Tijdens lading en ontlading gaan lithiumionen van de ene elektrode naar de andere. De bewegingsrichting verschilt afhankelijk van of de batterij wordt opgeladen of gelost, afhankelijk van de status van de batterij. Op het moment van lading en ontlading worden lithiumionen eindelijk ingebed in de atoomlaag van het elektrodenmateriaal, en dus hangt de capaciteit van de uiteindelijke batterij af van hoeveel materiaal kan herbergen van lithiumionen, dat wil zeggen, bepaald door het volume en de kwaliteit van de elektroden. 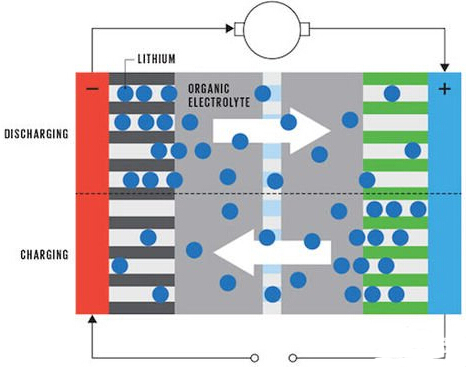
△ Lithium-ion batterij opladen en ontladen proces
Lithium-luchtbatterijen variëren. In metalen batterijen vindt een elektrochemische reactie plaats. Tijdens het ontladingsproces brengt de lithium-bevattende positieve elektrode lithiumionen vrij en bewegen de lithiumionen naar de negatieve elektrode en reageren met zuurstof op het oppervlak van de negatieve elektrode om lithiumperoxide te vormen (Li 2 O 2). Lithiumionen, elektronen en zuurstof reageren op het oppervlak van de negatieve elektrode gevormd door poreuze koolstof, omdat de chemische reactie niet optreedt op de negatieve elektrode en het lithiumion niet het negatieve elektrodenmateriaal is. Daarom zijn de capaciteit van de batterij en het volume of de massa van het negatieve elektrodenmateriaal niet te hoog. Grote relatie, zolang er voldoende oppervlakte is. Dat wil zeggen dat de capaciteit van de lithium-luchtbatterij niet wordt bepaald door het volume en de kwaliteit van de elektrode, maar het oppervlak van de elektrode. Dit is de reden waarom in een lithium-luchtbatterij een kleine massa-elektrode ook een grote hoeveelheid energie kan opslaan, wat resulteert in een hogere energiedichtheid. 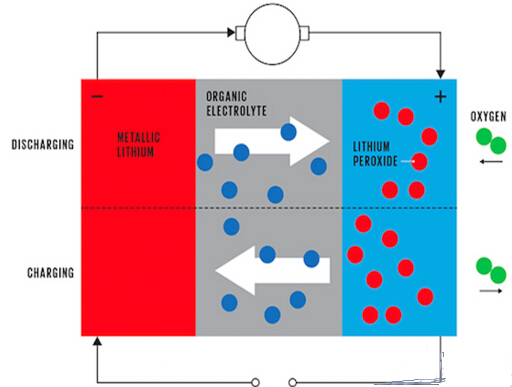
△ Lithium-Air batterij opladen en ontladen proces
Natuurlijk, naast energiedichtheid, zijn kosten ook een belangrijke overweging. De prijs van de batterij bevindt zich momenteel in het bereik van 200-300 US dollar / kWh, als u 5-6 km per kWh kunt draaien, heeft 800 km een batterij van 150 kWh nodig, u hebt 30.000-4,5 miljoen nodig. Een BMW 2 -serie auto heeft slechts $ 33.000 nodig. Daarom, als u de massaproductie wilt, moet de prijs per kWh onder $ 100 dalen. Welke problemen moet ik oplossen voor de commercialisering van de lithium-luchtbatterij? Wanneer het lithium en de zuurstof eenvoudig worden onderworpen aan een redox -reactie, is de theoretische maximale energiedichtheid die kan worden geproduceerd 3.460 WH/kg. Afgezien van het deel van de cel dat geen chemische reactie ondergaat, is de waarde van de energiedichtheid die uiteindelijk kan worden bereikt ook zeer wenselijk. Natuurlijk zul je ook problemen ondervinden. Het laadproces van een lithium-luchtbatterij is vergelijkbaar met dat van een conventionele lithium-ionbatterij, zolang deze extern onder druk staat. Het verschil is dat in een lithium-luchtbatterij, wanneer er een externe spanning is, de structuur van het lithiumperoxide wordt vernietigd en wordt gereduceerd tot zuurstof- en lithiumionen en de lithiumionen worden teruggebracht naar de positieve elektrode. Lithium-luchtbatterijen, zoals traditionele lithiumbatterijen, hebben meer laad- en ontladingscycli en hebben meer bijwerkingen in de batterij. Deze bijwerkingen zijn fundamenteel voor hun massaproductie en zelfs commercialisering. Om de effecten van deze bijwerkingen op de batterij te begrijpen, hebben we de elektrochemische massaspectrometer in het onderzoekscentrum gebruikt om de hoeveelheid door elke lading en ontladingscyclus te meten de hoeveelheid gas die wordt verbruikt en geproduceerd en geproduceerd. Als gevolg hiervan is een probleem ontdekt: de lithium-luchtbatterij stoott veel minder zuurstof uit tijdens het opladen dan de zuurstof die tijdens ontlading wordt verbruikt. (In de test wordt droge zuurstof gebruikt in plaats van lucht.) 
△ IBM Research Center's Elektrochemische massaspectrometer (: IBM)
In een ideale batterijcel is de zuurstof die wordt verbruikt tijdens ontlading gelijk aan de massa van zuurstof die wordt afgegeven tijdens het opladen. Maar de studie wees uit dat de hoeveelheid afgegeven zuurstof minder is, wat betekent dat de zuurstof die niet wordt vrijgegeven waarschijnlijk reageren met de componenten in de batterij -eenheid, zoals smelten in de elektrolyt, de batterij zit binnen. Consumptie. In een ander IBM-laboratorium in Zürich hebben we nieuwe experimenten uitgevoerd om deze zelfvernietigende chemische reactie te volgen en te automatiseren. Ten slotte werd de reden gevonden op de organische elektrolyt. Toen hebben we dit probleem bestudeerd. In de nieuwste batterij -eenheid, na het gebruik van een nieuwe elektrolyt, kan het het grootste deel van de zuurstof die tijdens ontlading wordt geabsorbeerd vrijgeven. Bovendien volgen we ook het verbruik en de productie van waterstof en water tijdens lading en ontlading, omdat de aanwezigheid van deze twee stoffen betekent dat er waarschijnlijk ten minste één zelf-consumptie-chemische reactie in de batterij is. Onze huidige batterij -eenheid heeft 200 laad- en ontladingscycli kunnen bereiken, hoewel dit is om het werkelijke laadproces veel minder te maken dan het theoretische maximum. Naast dit probleem hebben we enkele belangrijke bevindingen over de verschillende componenten van de lithium-luchtbatterij: 1. De positieve elektrode verschilt van de positieve elektrode gemaakt van grafiet in de traditionele lithium -ionbatterij. In de lithium-luchtbatterij zal de positieve elektrode die lithium bevat, een oppervlak veranderen tijdens het laadproces, en wat mosachtige of boomachtige structuur groeit. Het is een dendrite. Deze dendrieten zijn erg gevaarlijk omdat ze een geleidende lus kunnen vormen tussen de positieve en negatieve elektroden om een kortsluiting te creëren. 
△ Lithium-air batterij Positieve elektrode, na enkele tientallen cycli produceert het oppervlak dendritische structuur
Om het optreden van dendrieten te verminderen, hebben we een speciaal isolatiemembraan gebruikt. Deze separator bestaat uit een laag materiaal dat veel nanoschaalporiën bevat die klein genoeg zijn en gelijkmatig verdeeld over het membraan om doorgang van lithiumionen mogelijk te maken en dendritische productie te onderdrukken. Vanwege de aanwezigheid van deze separator blijft de anode glad na enkele honderden ladingscycli. Als een traditionele separator wordt gebruikt, zullen dendrieten na verschillende cycli plaatsvinden. Als u een glazen polymeer met geleidende ionen gebruikt, is het effect beter. 
△ Lithium-Air batterij Positieve elektrode, na gebruik van nano-isolatiefilm blijft het oppervlak glad
2. De elektrolyt die momenteel in de elektrolyt wordt gebruikt, reageert nog steeds met zuurstof of andere verbindingen geproduceerd in de lading- en ontladingscyclus en wordt dus verbruikt. Tot nu toe hebben we geen oplosmiddel gevonden dat stabiel genoeg is om de lithium-luchtbatterij het commerciële podium te laten betreden. 3. Tijdens het laadproces kunnen lithiumionen reageren met de negatieve elektrode om lithiumnitraat te produceren. Lithiumnitraat reageert ook met de elektrolyt, consumeert de elektrolyt en produceert koolstofdioxide. In de test hebben we ook de hoeveelheid geproduceerde lithiumnitraat gevolgd en namen we enkele maatregelen om de productie ervan te verminderen. Omdat de vereiste laadspanning echter met ten minste 700 mV hoger moet zijn dan de bedrijfsspanning van de batterij. Overspanning zal de oplaadefficiëntie van de batterij verminderen. We hebben geprobeerd koolstof om te zetten in sommige andere metaaloxiden en de resultaten zijn niet veel veranderd. 4. Katalysatoren met betrekking tot het al dan niet gebruiken van katalysatoren in metalen batterijen, er zijn veel debatten geweest tussen de profs en de tegenstanders. Het gebruik van een katalysator kan het optreden van overdrukomstandigheden aanzienlijk verminderen, maar dezelfde katalysator zal in het algemeen ook het verbruik van elektrolyt versnellen. In onze theoretische studies is de activeringsenergie zeer laag in de oxidatie en vermindering van lithium. Daarom is de katalysator in lithium-luchtbatterijen niet nodig. 5. Bereiding van lucht hoewel de batterij een lithiumluchtbatterij wordt genoemd, gebruiken we in feite droge zuurstof. De nadruk wordt gelegd op "drogen" omdat het alleen nodig is om de componenten van waterdamp en koolstofdioxide in de lucht te verwijderen. Om dergelijke lucht in commerciële batterijen te produceren, is een licht, efficiënt en stabiel luchtzuiveringssysteem nodig. Vanuit dit perspectief kan de praktische toepassing van lithium-luchtbatterijen zich in bussen, vrachtwagens en andere grote voertuigen bevinden. Alleen deze grote voertuigen zijn geschikt voor luchtzuiveringsapparatuur. De batterijeenheid die momenteel wordt gebruikt voor het testen is nog steeds klein in grootte, een diameter van 76 mm en 13 mm lang, wat verre van genoeg is voor de standaard van elektrische voertuigen. Dus een van de belangrijkste taken die moeten worden gedaan, is hoe u grotere batterijcellen kunt maken, veel batterijcellen in één batterijpakket kunt verpakken en vervolgens een batterijbeheersysteem kunt hebben. We testen ook enkele verschillende maten, zoals 100 x 100 mm (100 mm diameter, 100 mm lengte). Momenteel bevindt dit project zich nog steeds in het eerste basiswetenschappelijke stadium van materialen en chemische reacties, maar de verkregen resultaten zijn positief. In onze studie is de energiedichtheid die nu kan worden bereikt, lithiumoxidoreductieve reactie van 15 kWh/kg (met behulp van een rauwe koolstofkathode, 5700 mAh x 2,7 V/g), en de energiedichtheid in de cel is ongeveer 800 wh/kg . Natriumbatterij: lage energiedichtheid, maar in stabiele metalen luchtbatterijen zijn er veel metalen die kunnen worden gebruikt, naast lithium, natrium en kalium. De omgekeerde reactie van deze metalen is eenvoudiger, en relatief zwaardere metalen zoals magnesium, aluminium, zink, ijzer, enz. Blijken moeilijk op te laden te zijn, dus het Battery 500 -project heeft ervoor gekozen om zowel lithium als natrium te bestuderen. metaal. Natriumbatterijen zijn een andere interessante combinatie, hoewel de bereikte energiedichtheid lager is in vergelijking met lithium-luchtbatterijen, maar de voordelen zijn stabieler. De reden waarom de energiedichtheid laag is, is dat de gegenereerde chemische reactie anders is. Zoals hierboven vermeld, reageert in lithium-luchtbatterijen lithium met zuurstof om lithiumperoxide (Li2O2) te produceren, maar in natriumbatterijen reageert natrium met zuurstof met slechts één elektron, wat resulteert in natriumsuperoxide NaO2. In plaats van natriumperoxide, Na2O2. Ter vergelijking: de energiedichtheid die een natriumbatterij kan produceren, wordt theoretisch verminderd met de helft, en de theoretische bovengrens van energiedichtheid is 1100 WH/kg. Aan de andere kant zijn natriumbatterijen efficiënter dan lithium-luchtbatterijen en de overspanning is vrij laag, minder dan 20 mV (700 mV voor lithium). Gezien hiermee kan de bedrijfsspanning van de batterij-eenheid worden gereduceerd tot 3V, zodat het zelf-consumptie van andere componenten in de batterij veel kan worden verminderd, zoals elektrolyt. We hebben het gemeten door experiment en hebben het geverifieerd. Dit heeft het voordeel dat de stabiliteit van de batterij vrij hoog is, en de capaciteit van de batterij verandert nauwelijks na 50 lading- en ontladingscycli. Er zijn ook enkele uitdagingen in het commerciële gebruik van natriumbatterijen. Een natrium-luchtbatterij verbruikt bijvoorbeeld twee keer zoveel zuurstof als een lithium-luchtbatterij in reactie op een reactie, gelijk aan de hoeveelheid lucht die nodig is om een zuigermotor van hetzelfde vermogen te produceren. Bovendien is de chemische activiteit van natriummetaal vrij hoog, en veel mensen zullen de demonstratie van de leraar scheikunde in het klaslokaal van de middelbare school herinneren. Een klein stuk natrium wordt in het water gegooid en er zal een gewelddadige chemische reactie optreden. Lithium is echter een zeldzaam metaal en het is niet goedkoop. Maar natrium is een gewoon metaal en de kosten zijn extreem laag. De kosten van materialen in dezelfde maat natrium-luchtbatterij zijn minder dan een tiende van die in lithium-luchtbatterijen. Hoewel op de lange termijn lithium-luchtbatterijen betere prestaties zullen hebben, maar gezien de stabiliteit en kosten, is de natrium-luchtbatterij die niet zo laag is als de energie een betere keuze is van de huidige batterij naar de toekomst. 0 keer
Window._bd_share_config = {"gemeenschappelijk": {"bdsnSkey": {}, "bdtext": "", "bdmini": "2", "bdminilist": "bdpic": "", "bdstyle": " 0 "," bdsize ":" 24 "}," share ": {}," image ": {" viewList ": [" qzone "," tsina "," tqq "," Renren "," Weixin "], "ViewText": "Delen op:", "Viewsize": "16"}, "SelectShare": {"BdContainerClass": NULL, "BDESelectminilist": ["Qzone", "Tsina", "Tqq", "Renren" , "weixin"]}}; met (document) 0 [(getElementsByTagName ('head') [0] || body) .AppendChild (createElement ('script')). src = 'http: //bdimg.share. Baidu.com/static/api/js/share.js?v=89860593.js?cdnversion= ' + ~ (-new date ()/36e5)];







